FUTIBATINIB được FDA phê duyệt( 9/2022) cho chỉ định để điều trị ung thư Đường Mật
23/10/2025 14:35:49
Cơ chế tác dụng
Futibatinib là một chất ức chế (inhibitor) không hồi phục (irreversible) của các thụ thể fibroblast growth factor receptor (FGFR) – bao gồm FGFR1, FGFR2, FGFR3 và FGFR4.
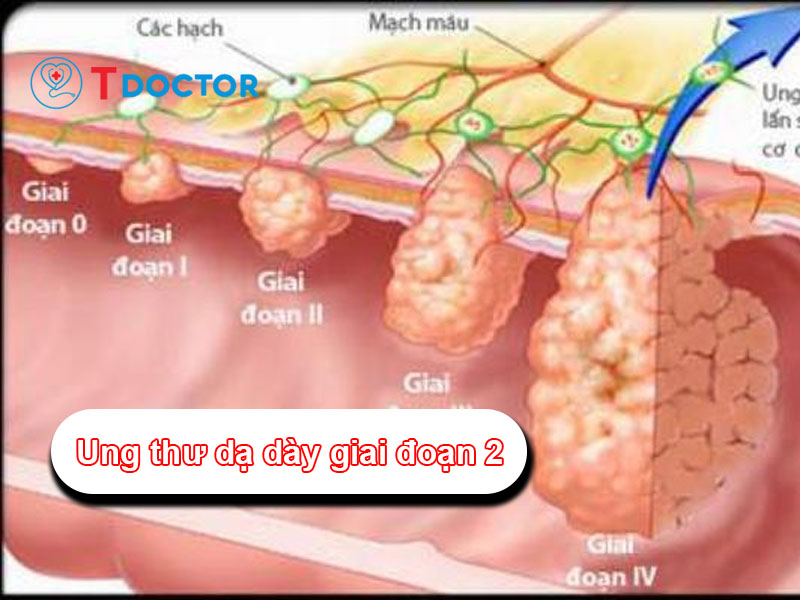
Với ung thư đường mật có tái sắp xếp FGFR2, việc ức chế con đường tín hiệu FGFR giúp ngăn chặn tăng sinh tế bào ung thư và giảm khả năng nhân lên/lan tràn của khối u.
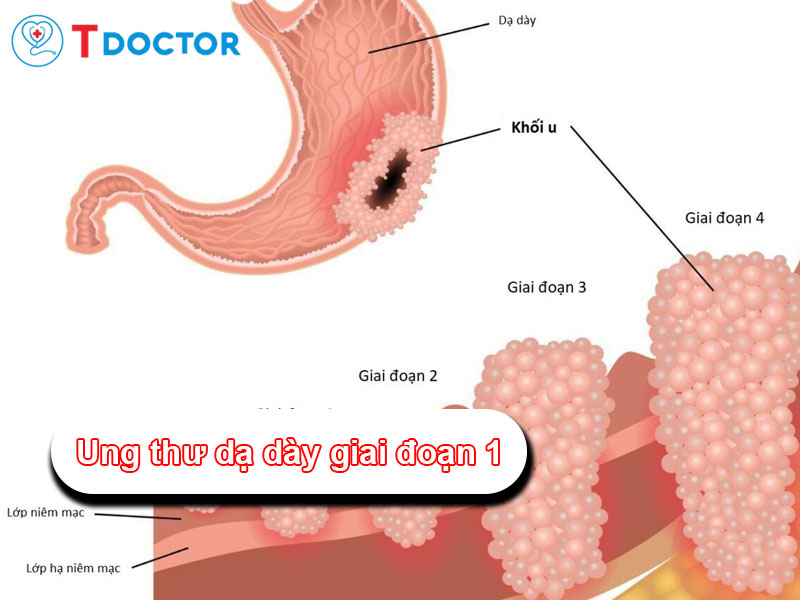
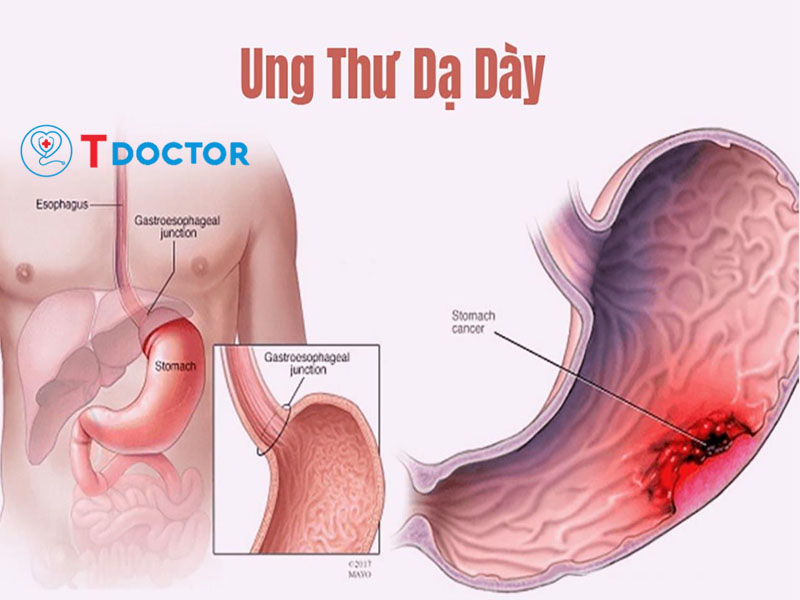
FUTIBATINIB được FDA phê duyệt( 9/2022) cho chỉ định để điều trị ung thư Đường Mật, không thể phẫu thuật cắt bỏ, di căn hoặc tiến triển tại chỗ đã được điều trị trước đó, ở bệnh nhân trưởng thành có tái sắp xếp / dung hợp gen FGFR2 (fibroblast growth factor receptor 2).
Futibatinib là một chất ức chế FGFR1, 2, 3 và 4 phân tử nhỏ đang được nghiên cứu, uống, mạnh, chọn lọc và không thể đảo ngược. Nó hiện đang được phát triển như một phương pháp điều trị cho các khối u rắn tiên tiến có gen FGFR1-4 bất thường. Một phương pháp điều trị tiềm năng cho bệnh nhân (bao gồm cả ung thư đường mật). Trong các khối u mang gen FGFR1-4 quang sai, futibatinib có thể liên kết một cách chọn lọc và không thể đảo ngược với túi liên kết ATP của FGFR1-4, dẫn đến ức chế các con đường dẫn truyền tín hiệu qua trung gian FGFR, giảm sự tăng sinh tế bào khối u và sự chết của tế bào khối u.
Futibatinib được phê duyệt dựa trên kết quả hiệu quả và an toàn của nghiên cứu FOENIX-CCA2 giai đoạn 2. Kết quả cho thấy tỷ lệ đáp ứng mục tiêu (ORR) của điều trị futibatinib là 37,3%, thời gian đáp ứng trung bình (DOR) là 8,3 tháng, kiểm soát bệnh sau khi theo dõi ≥6 tháng Tỷ lệ (DCR) là 82%. Đặc biệt, sự thuyên giảm điều trị được quan sát thấy ở tất cả các phân nhóm về đặc điểm cơ bản (bao gồm tuổi, giới và các liệu pháp toàn thân trước đó), bao gồm cả người già ≥65 tuổi (ORR=57%; n=8/14). Trong quá trình nghiên cứu, các tác dụng phụ của futibatinib có thể kiểm soát được.
Chỉ định phê duyệt
Chỉ định đã được FDA phê duyệt:
Người lớn (≥ 18 tuổi)
Ung thư đường mật trong gan (intrahepatic cholangiocarcinoma – iCCA), không thể phẫu thuật hoặc đã di căn, hoặc bệnh tiến triển tại chỗ.
Khối u mang FGFR2 gene fusions hoặc các rearrangements khác xác định qua xét nghiệm gen.Bệnh nhân đã được điều trị trước bằng một hoặc nhiều liệu pháp hệ thống.
Approval là “accelerated” (rút gọn) — việc duy trì chỉ định có thể phụ thuộc vào kết quả thêm từ các nghiên cứu xác nhận.
-
 ...
...Băng keo liên kết (l/10cuộn)
-
 ...
...Panadol Extra With Optizorb Gsk (H/120v)
-
 ...
...Mekocefaclor Cefaclor 500mg Mekophar (H/16v)
-
 ...
...Disolvan Bromhexine 0.8mg/Ml Mekophar (C/100ml)
-
 ...
...Meko Coramin Mekophar (H/20v)
-
 ...
...Pexate 500mg điều trị ung thư
-
 ...
...Geftib 250 điều trị ung thư
-
 ...
...Men tiêu hóa menpeptine Enzyme
-

SP CHÍNH HÃNG
Đa dạng và chuyên sâu
-

ĐỔI TRẢ TRONG 30 NGÀY
kể từ ngày mua hàng
-

CAM KẾT 100%
chất lượng sản phẩm
-

MIỄN PHÍ VẬN CHUYỂN
theo chính sách giao hàng

Xem danh sách nhà thuốc trên toàn quốc

-

Duy Nguyễn Nhất





Rất tuyệt vời, đặc biệt trong mùa dịch đi lại khó khăn. Chúc tdoctor ngày càng phát triển và mở rộng phạm vi ra nhiều tỉnh hơn, nhất là vùng Đồng bằng sông Cửu Long.
-

Quốc Bình Vũ





Ứng dụng rất hay. Giúp mọi người hạn chế bệnh gì cũng phải đến bệnh viện khám. Đỡ mất thời gian, công sức và tiền bạc vì nhiều khi vô gặp bs cũng chỉ cần hỏi vài câu và cho SP.
-

Nguyễn Ngọc Minh





Em bị ung thư thấy bác sĩ tuyến trung ương trong hệ thống tdoctor, bác sĩ bên tdoctor rất nhiệt tình, rất tiện cho trường hợp mua sản phẩm dược và thực phẩm chức uy tín online.